小肠是吸收营养的主要器官,其广泛切除会导致吸收不良和消瘦,这被称为短肠综合症(SBS)。类器官技术可以在体外有效地扩大肠道上皮组织,但是整个小肠的重建(包括复杂的淋巴血管系统)仍然具有挑战性。在这里,科研人员通过用回肠衍生的类器官替代天然结肠上皮细胞来生成功能性小肠结肠(SIC)。他们首先发现异种移植的人类回肠类器官保持它们的区域特征并在小鼠结肠中形成新生的绒毛结构。在类器官单层的体外培养中,进一步揭示了腔内机械流在绒毛形成中的重要作用。然后,通过将SIC重新定位在回盲肠交界处来开发大鼠SIC模型,在回盲肠交界处,上皮暴露于恒定的腔内肠液流。这种解剖学上的重定位为SIC提供了小肠的器官结构,包括完整的脉管和神经支配,绒毛结构和乳腺(特定小肠吸收脂肪的淋巴结构)。虽然结肠类器官而不是回肠类器官的移植总是导致死亡,但是, SIC具有吸收功能,在SBS大鼠模型中可显着改善肠道衰竭。这些实验数据为用于再生目的肠类器官的原理提供了证据,并为SBS治疗提供了可行的策略。
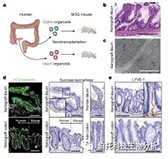
异种移植的人类回肠类器官在小鼠结肠中重建绒毛结构
a,用于将人回肠或结肠类器官移植到免疫缺陷(NOG)小鼠结肠的工作流程。
b,移植的人类回肠上皮的苏木精和曙红染色。
c,异种移植的人回肠上皮的透射电子显微镜图像。
d,异种移植回肠和结肠上皮中人角蛋白(hCytokeratin)和蔗糖酶-异麦芽糖酶的染色。人体组织样本的染色显示在右侧,以供参考。
e,人回肠和结肠异种移植物中LYVE-1表达的免疫组织化学。
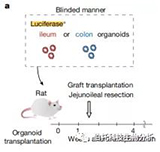
盲法移植回肠或结肠类器官的实验策略
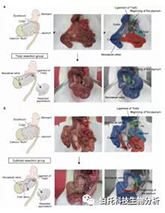
在大鼠中进行空肠切除的手术程序
图和图像显示了空肠切除术的全部(a)和部分(b)。大肠切除组保留了3 cm的回肠末端。白色箭头表示吻合部位。
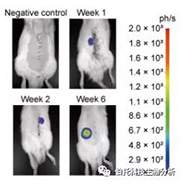
回肠类器官移植大鼠的代表性生物发光图像,显示萤光素酶阳性移植物的稳定植入。
文章链接:https://www.nature.com/articles/s41586-021-03247-2
